3- Propriedades periódicas
Propriedades aperiódicas - Os valores somente crescem ou decrescem à medida que aumenta o número atômico. Exemplos:massa atômica e calor específico.
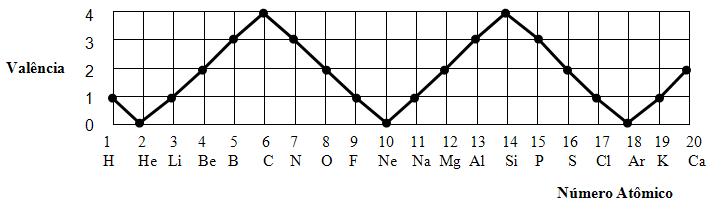
Propriedades periódicas - São aquelas cujos valores numéricos crescem ou decrescem em função do número atômico crescente.
Vejamos as principais propriedades periódicas:
Raio atômico – O raio de um átomo é uma propriedade difícil de ser determinada, pois a eletrosfera de um átomo não tem fronteira definida.
O raio atômico de um elemento depende de dois fatores:
a) Número de níveis eletrônicos (camadas): numa família, quanto maior o número atômico, maior é o raio atômico.
b) Carga nuclear (número atômico): num período, quanto maior o número atômico, menor é o raio atômico.
ionização.
Li(g) ® Li+(g) + 1e- 1.ºPI = 124kcal/mol
Li +(g) ® Li++(g) + 1e- 2.ºPI = 1744kcal/mol
Li ++(g) ® Li+++(g) + 1e- 3.ºPI = 2823kcal/mol
1.º PI < 2.º PI < 3.º PI <...
Eletronegatividade – É a propriedade pela qual o átomo apresenta maior tendência a ganhar elétrons. Esta propriedade depende de dois fatores: número de elétrons na última camada e tamanho do átomo.
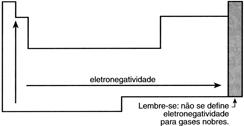
O cientista Linus Pauling propôs uma escala de valores para a eletronegatividade:
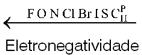
Eletropositividade – É a propriedade pela qual o átomo apresenta maior tendência a perder elétrons. Evidentemente, esta propriedade é o inverso da eletronegatividade.
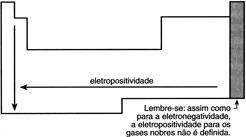
Vejamos as principais propriedades periódicas:

O raio atômico de um elemento depende de dois fatores:
a) Número de níveis eletrônicos (camadas): numa família, quanto maior o número atômico, maior é o raio atômico.
b) Carga nuclear (número atômico): num período, quanto maior o número atômico, menor é o raio atômico.

Raio Iônico - Para íons isoeletrônicos (iguais números de elétrons), o de menor número atômico será o maior, pois apresenta menor atração entre o núcleo e os elétrons.
8O2- > 9F1- > 11Na1+ > 12Mg2+
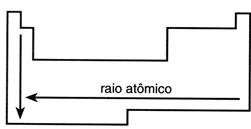
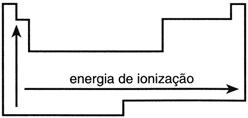
Potencial de ionização – É a energia necessária para remover um elétron de um átomo isolado no estado gasoso. À medida que aumenta o tamanho do átomo, aumenta a facilidade para a remoção de um elétron de valência. Portanto, quanto maior o tamanho do átomo, menor o potencial deionização.

Li +(g) ® Li++(g) + 1e- 2.ºPI = 1744kcal/mol
Li ++(g) ® Li+++(g) + 1e- 3.ºPI = 2823kcal/mol
1.º PI < 2.º PI < 3.º PI <...
Eletronegatividade – É a propriedade pela qual o átomo apresenta maior tendência a ganhar elétrons. Esta propriedade depende de dois fatores: número de elétrons na última camada e tamanho do átomo.

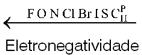

Nenhum comentário:
Postar um comentário